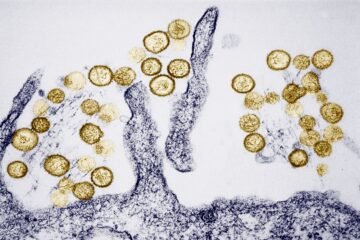
La atención mediática sigue pendiente del MV Hondius, el buque donde se detectó un brote de hantavirus que ya ha infectado a diez personas y ha matado a tres. Pero la reconstrucción científica de los hechos, el análisis genómico de los virus, se está desarrollando lejos de los focos, en pequeños laboratorios de todo el mundo. Microbiólogos en Sudáfrica, Suiza y Países Bajos están secuenciando distintas muestras del virus, abriendo las cajas negras de estos organismos para entender qué pasó en el barco y cómo se comporta esta cepa. Sus primeras conclusiones ya están llegando.
Distintos laboratorios han secuenciado parcialmente el genoma del virus de varios infectados y son casi idénticos, lo que ratifica la idea de la transmisión entre humanos
La atención mediática sigue pendiente del MV Hondius, el buque donde se detectó un brote de hantavirus que ya ha infectado a diez personas y ha matado a tres. Pero la reconstrucción científica de los hechos, el análisis genómico de los virus, se está desarrollando lejos de los focos, en pequeños laboratorios de todo el mundo. Microbiólogos en Sudáfrica, Suiza y Países Bajos están secuenciando distintas muestras del virus, abriendo las cajas negras de estos organismos para entender qué pasó en el barco y cómo se comporta esta cepa. Sus primeras conclusiones ya están llegando.
Un análisis comparado de cinco infectados por el hantavirus ha confirmado que hubo contagio entre personas. “Los genomas virales son prácticamente idénticos”, explica en un intercambio de mensajes Blas Oude Munnik, virólogo del Centro Médico de la Universidad Erasmus en Róterdam y coautor del estudio, que se ha publicado en la plataforma abierta Viriological. Esto significa que, tras un contagio de ratón a humano, “lo más probable es que el virus se propagara de persona a persona a bordo del crucero”.
Esta información coincide con la que sugería la reconstrucción de los hechos. Los primeros infectados, un matrimonio de holandeses, habían recorrido el cono sur de América durante meses, pasando por zonas donde viven los ratones colilargos, reservorio principal del virus. El hombre falleció el 11 de abril, la mujer el 26 o 27. A partir de entonces, varios pasajeros empezaron a mostrar síntomas. La cronología de las infecciones, así como la ausencia de roedores y casos documentados en Tierra de Fuego, de donde partió el barco, hicieron pensar a las autoridades que ellos fueron los primeros infectados y que pasaron después el virus al resto del pasaje. Pero hasta ahora no había una confirmación científica de esta hipótesis.
“Los datos genómicos no pueden excluir la posibilidad de que la exposición ambiental inicial involucrara a más de un pasajero infectado de la misma fuente”, matizan los expertos. “Resolver esto requerirá datos epidemiológicos adicionales”. Puede que solo el hombre fuera el infectado original o puede que se infectara junto a su mujer. Se da también la circunstancia de que todavía no se ha analizado el virus que le infectó a él. “Falleció hace algún tiempo, cuando no sabíamos que había un brote de hantavirus”, justifica Munnik.
El análisis se basa en cuatro secuenciaciones parciales, de dos pacientes en Johannesburgo y otros dos en Países Bajos. También en un secuenciado genómico total del virus, del paciente que se encuentra hospitalizado en Suiza. Este análisis, el primero completo, ya confirmó que se trataba de la variante Andes y descartó mutaciones del virus, que era algo que preocupaba a los expertos. Los otros cuatro análisis parciales confirman esta idea.
“El diagnóstico lo hicimos con una PCR específica para el hantavirus Andes el martes pasado”, explica Pérez-Rodríguez sobre el análisis del virus del paciente de Suiza. “La secuencia también es útil porque permite concluir que los tests de laboratorio basados en la detección del genoma del virus Andes (PCR) deberían ser capaces de detectar el virus”.
El virus de Suiza fue secuenciado mediante tecnología Illumina, que identifica mutaciones, variantes y realiza una secuencia completa del virus. Compararon los tres segmentos en los que se divide el virus. “Y se vio que no ha habido reagrupamiento, es decir, intercambio de segmentos entre cepas que dan lugar a un nuevo virus”, cuenta Pérez-Rodríguez. Con estos datos se puede descartar una mutación, que era lo que más preocupaba a los expertos. “La secuencia se agrupa estrechamente con aislados de Andes ya descritos, especialmente con los de Argentina 2018–2019, lo que sugiere que no es una variante muy divergente ni una cepa totalmente nueva”, explica Estanislao Nistal Villán, investigador del grupo de virología de la Universidad CEU San Pablo.
Los casos que menciona Nistal son los de un brote que se dio en la Patagonia y que sorprendió a la comunidad científica por su alto contagio, que se inició en un cumpleaños. Hubo 34 infecciones y 11 muertos. Fue un análisis genético de estos casos el que demostró que la cepa Andes puede contagiarse entre humanos (el resto de variantes solo saltan de los ratones a personas). Esto fue una relativa sorpresa para un virus del que se conoce poco (hay menos de mil casos registrados y estudiados) y con una variabilidad muy amplia.
El hantavirus es un patógeno con poca capacidad de mutación, a diferencia de lo que sucede con otros virus como el de la gripe o el coronavirus. Esta cepa, de hecho, guarda mucha similitud (con tasas que rondan el 98%) con las detectadas en humanos en Argentina en 1997 y 2018. El virus apenas ha cambiado en 30 años. El presente informe ha encontrado solo dos mutaciones genuinas en toda la secuencia, “ambas sin consecuencias funcionales”, explican los autores, es decir, que no hace al virus ni más ni menos peligroso.
El brote de hantavirus ha tenido una dimensión internacional. Su gestión ha requerido de la cooperación entre organismos supranacionales como la OMS, nacionales como España y Holanda, y autonómicos, como el Gobierno de Canarias. Pero si bien la cooperación entre estos ha evidenciado ciertos roces; a nivel científico, la coordinación ha sido total. “Los laboratorios participantes fueron convocados con anticipación para intercambiar datos y evaluar cómo las diferencias en las plataformas de secuenciación […] podrían afectar”, explican los autores. Se han usado diferentes plataformas de secuenciación genómica, pero los autores han resuelto el problema que esto podía suponer. “Resulta difícil comparar los datos con precisión si no se tiene acceso a los archivos de datos originales”, concede Munnik. “Pero compartimos estos archivos entre nosotros y, por lo tanto, podemos llegar a conclusiones sólidas”.
En el momento de este informe, continúan los esfuerzos de secuenciación para subsanar las deficiencias y completar el análisis de estos primeros casos, explica. “Por lo tanto, estos hallazgos […] podrían actualizarse a medida que se disponga de datos adicionales”.
Ciencia en EL PAÍS